¿Funciona el trasplante fecal?
Una estrategia para manipular la microbiota es sustituirla o reemplazarla por completo, en vez de añadir un microorganismo (probiótico) o un nutriente (prebiótico). En los últimos años se está hablando mucho del trasplante de la microbiota intestinal completa de una persona sana a otra con una enfermedad, es lo que se ha llamado el trasplante fecal o FMT (Faecal Microbiota Trasplantation, en inglés). Si, ya sé que esto suena francamente asqueroso porque en definitiva es un trasplante de caca, pero el objetivo del trasplante fecal es restaurar los microbios de nuestro intestino. En realidad el trasplante fecal es un tipo de bacterioterapia, emplear bacterias para curar una enfermedad.
Para combatir al difícil y puñetero Clostridium difficile*
Es muy frecuente que tras un tratamiento fuerte con antibióticos nuestras bacterias intestinales también se resientan y se altere la diversidad microbiana, incluso durante meses, y esto puede permitir que otras bacterias potencialmente patógenas proliferen. Esto es lo que ocurre en las infecciones por Clostridium difficile: los antibióticos reducen la diversidad de bacterias intestinales, lo que favorece la esporulación y germinación de las esporas de Clostridium difficile (un patógeno oportunista que llevamos en nuestras tripas) y la consiguiente producción de enterotoxinas que dañan el epitelio intestinal y causan inflamación y diarrea. En algunos casos la diarrea es intensa, causa fiebre y dolor abdominal, y puede llegar a ser crónica, muy grave e incluso mortal. Algunas cepas de Clostridium difficile son especialmente puñeteras y el tratamiento suele consistir en más antibióticos, como la vancomicina. Desgraciadamente, en aproximadamente el 25% de los pacientes no es efectivo y sufren diarreas recurrentes que hacen la vida de los pacientes muy incómoda y difícil.
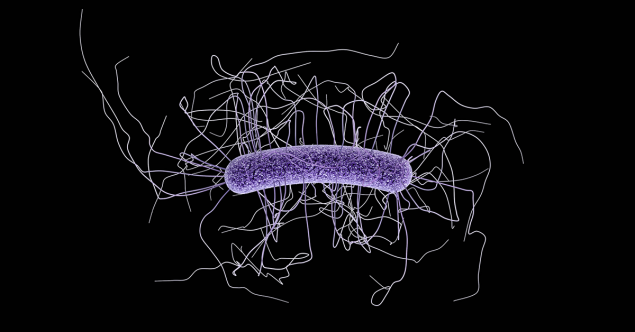
(Fuente: CDC)
Para estos casos concretos, la solución puede ser el trasplante fecal. Para ello, se prepara una solución con heces de donantes sanos voluntarios, que contienen la comunidad completa de microbios intestinales. Dentro de las seis horas posteriores a su obtención, la solución se introduce mediante un tubo nasoduodenal a los pacientes durante 30 minutos, a un ritmo de unos 50 mililitros cada 2-3 minutos (también se han empleado enemas, colonoscopias, incluso píldoras para introducir los nuevos microbios). Previamente, las heces se han analizado para asegurarse que no contengan ningún parásito, ni bacterias o virus patógenos.
El tratamiento de la infección recurrente por Clostridium difficile que no responde a antibióticos es la única indicación clínica para la que está aprobado el trasplante fecal
En el caso concreto de infecciones recurrentes por Clostridium difficile los resultados del trasplante fecal suelen ser espectaculares: el 94% de los pacientes tratados con heces de donantes sanos se curan, frente a sólo el 28% de los que reciben antibióticos. Los efectos secundarios del trasplante suelen ser mínimos (bueno, … sigue leyendo): diarrea inmediatamente después del tratamiento y algunos dolor de tripas, pero los síntomas desaparecen pocas horas después del trasplante. En algún caso se ha descrito que el receptor ha engordado después del trasplante quizá porque el donante era obeso. Aunque suena muy mal lo del trasplante fecal, funciona. La administración de heces de donantes sanos a pacientes con infecciones recurrentes de Clostridium difficile resulta ser un tratamiento mucho más efectivo que los antibióticos. Parece ser que a Clostridium eso de estar bien acompañado por una multitud de otros microbios “buenos” no le sienta bien.
¿Cómo “funciona” el trasplante fecal?
El éxito que está teniendo el trasplante fecal en el tratamiento de la infección por Clostridium difficile ha generado mucho interés en emplearlo en otras enfermedades. Sin embargo, hasta la fecha este éxito no ha podido ser replicado para otras dolencias, como la enfermedad inflamatoria intestinal, el síndrome colon irritable o la obesidad. Por eso, hay que ser muy cautos. Antes tenemos que entender cuáles son los mecanismos por los que el trasplante fecal funciona en estos casos de infección recurrente por Clostridium difficile (1).
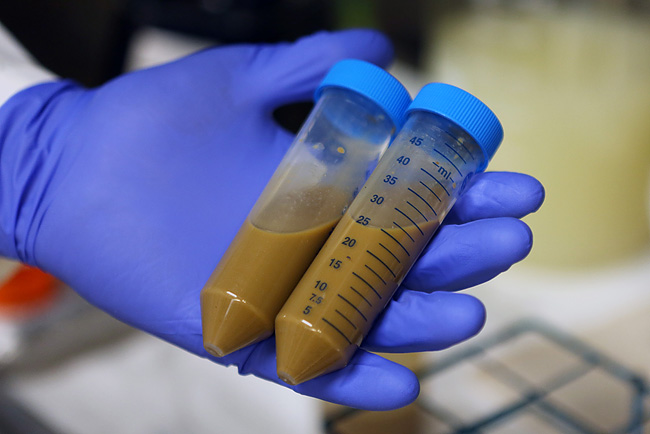
Se ha comprobado que la infección por Clostridium difficile genera una drástica alteración de la diversidad de la microbiota: desaparecen casi completamente los Bacteroidetes, se reducen los Firmicutes y hay un aumento masivo de Proteobacterias. En estos casos, el trasplante fecal lo que hace es restaurar las funciones normales de la microbiota intestinal. Algunos han propuesto erróneamente que con un probiótico de microorganismos “buenos” se puede corregir este tipo de disbiosis tan severa. Lo que se comprueba es que solo una intervención con una comunidad microbiana compleja que ha sido optimizada por co-evolución con su huésped sano (esto es el trasplante fecal) es capaz de restaurar la microbiota funcional. (Para más información sobre los probióticos puedes consultar Manipular la microbiota (I): probióticos si, probióticos no.)
En condiciones normales, la microbiota intestinal indígena es un complejo ecosistema, que puede competir con Clostridium difficile por el mismo nicho ecológico y nutrientes. Es como si estuviéramos en una gran auditorio con todas las butacas ocupadas por “residentes”. Si aparece el Clostridium patógeno, todo está ocupado, no hay sitio ni alimentos disponible. En esas condiciones Clostridium no puede asentarse, no puede colonizar el intestino. Pero además, la competición no se limita al espacio y los nutrientes, si no que algunas especies de la microbiota normal son capaces de producir bacterocinas, pequeños péptidos con acción bactericida contra Clostridium.
Sabemos también que el metabolismo de los ácidos biliares influye en la colonización de Clostridium. Los ácidos biliares, y sus derivados, son productos del metabolismo del colesterol. Además de su papel en la digestión y absorción de los lípidos, los ácidos biliares tienen otros efectos fisiológicos en el metabolismo y la respuesta inmune. Los ácidos biliares primarios se producen en el hígado y luego son modificados por la microbiota intestinal en el colon para producir los ácidos biliares secundarios. Estos pueden tener efectos sobre la propia microbiota y pueden estimular e inhibir el crecimiento de Clostridium difficile. Por ejemplo, algunos ácidos biliares primarios (como el ácido cólico) pueden promover la germinación de esporas de Clostridium, mientras que otros ácidos biliares secundarios (como el ácido litocólico) tienen el efecto contrario. En personas sanas, la microbiota indígena mantienen un equilibrio entre los distintos ácidos biliares que inhiben a Clostridium difficile. Sin embargo, en condiciones de disbiosis, aumentan los ácidos biliares primarios que estimulan la germinación de Clostridium difficile. El trasplante fecal lo que haría entonces es restaurar el metabolismo de ácidos biliares, sobre todo los secundarios, de forma que se inhibiera le germinación de las esporas de Clostridium difficile.
Otro posible efectos del trasplante fecal es la de restaurar la barrera intestinal, por regenerar el epitelio, favorecer la producción de moco protector, de péptidos antimicrobianos específicos contra los patógenos, o de mediadores anti-inflamatorios.
Los “super-donantes” de heces
Algunas dudas que yo mismo tenía sobre todo esto del trasplante fecal es cómo hacerse donante de muestras y si todo el mundo vale para ser donante. Si buscas en internet verás que ya hay algunas empresas en EE.UU. y en Europa donde puedes donar tus muestras, te pagan por ello y encima te dicen que ¡tus heces salvan vidas!

El trasplante fecal ha sido ensayado también para otras afecciones más complejas y distintas a la infección por Clostridium: enfermedad inflamatoria intestinal, colitis alérgica, enfermedades hepáticas, metabólicas e incluso neurológicas. Sin embargo, en estos otros casos los resultados son mucho más modestos y variables, muy dependientes de las características de la muestra del donante. Estos resultados sugieren que los donantes no son todos iguales, y que pueden existir algunos “super-donantes” cuyas muestras fecales sean más eficaces (2).
La diversidad microbiana del donante es uno de los factores más
influyente en el éxito del trasplante fecal
En concreto, se ha comprobado que las heces ricas en bacterias de las familias Ruminococcaceae y Lachnospiraceae (los géneros Roseburia, Oscillibacter, Blautia, Dorea) son las mejores para que un trasplante fecal funcione. Estas bacterias son buenas productoras de butirato, un tipo de ácido graso de cadena corta que modula la respuesta inmune. Sin embargo, el éxito del trasplante fecal no solo depende del donante sino también del receptor: al final, como el cualquier trasplante, debe existir cierta compatibilidad entre las comunidad microbianas de ambos. Parece ser que la respuesta al trasplante fecal depende sobre todo de la capacidad de la microbiota del donante de restaurar el desajuste metabólico específico asociado con cada enfermedad particular. Según esto, se debería primero identificar que alteración metabólica concreta tiene cada paciente, para luego proponerle un donante concreto con la muestra enriquecida en aquellas bacterias que mejor le vayan para su caso particular. En definitiva, no toda caca vale, el trasplante fecal deber ser “personalizado”.
Ojo: posibles efectos secundarios
Hace unos meses fue noticia que la Agencia del Medicamento de EE.UU. (la FDA por sus siglas en inglés) había suspendido los ensayos clínicos de trasplantes fecales después de que dos pacientes contrajeron infecciones graves debido a que los trasplantes contenían bacterias resistentes a los antibióticos, lo que provocó la muerte de uno de ellos (Ver alerta de la FDA).

El caso concreto era de dos paciente inmunocomprometidos que recibieron un trasplante fecal del mismo donante. En las heces del donante había un Escherichia coli portador de beta-lactamasas que le hacía ser multirresistente a los antibióticos (ya es mala suerte), lo que les causó una infección invasiva. Uno de ellos murió. Las muestras del donante no había sido analizadas previamente para comprobar la existencia de este tipo de bacterias resistentes. A partir de este caso la FDA ha determinado que se deben realizar determinados análisis de las muestras fecales antes de poder emplearlos para el trasplante, y de que hay que alertar a los pacientes del riesgo que supone este tipo de tratamientos. Un trasplante fecal también tiene riesgos, es algo muy serio y solo debería realizarse en un entorno clínico y seguro.
El futuro
El trasplante fecal está todavía en su infancia. Parece que funciona bien en algunos casos de infección por Clostridium difficile, pero ese éxito no puede ser extrapolado a otras dolencias. No sabemos todavía si al trasplantar los microbios también se puede producir un desajuste en esos compuestos como neurotransmisores y neuromoduladores que están asociados a la microbiota intestinal. Hace falta más investigación. No hay protocolos óptimos y consensuados que aseguren que la microbiota trasplantada realmente se ha “injertado” en el receptor. Tampoco sabemos cuál sería la microbiota perfecta o idónea para cada dolencia y para cada paciente. Es necesario estandarizar las técnicas y protocolos, evaluar su efectividad clínica. Pero no podemos descartar que en el futuro esta forma de bacterioterapia (suena así mucho mejor) se incluya en los tratamientos de algunas enfermedades, o incluso que depositemos nuestras propias muestras en “bancos” de heces para un auto-trasplante de microbiota intestinal.
* Clostridium difficile ahora se denomina Clostridioides difficile.
Para saber más:
(1) Understanding the mechanisms of faecal microbiotatransplantation. Khoruts, A., y col. Nat Rev Gastroenterol Hepatol. 2016. 13(9):508-16.
(2) The super-donor phenomenon in fecal microbiota transplantation. Brooke C. Wilson, B.C., y col. Front. Cell. Infect. Microbiol.| 2019. 9:2.