Diseñan un nuevo compuesto capaz
de restaurar la susceptibilidad a los carbapenems
El problema
La extensión de bacterias
resistentes a los antibióticos es un problema mundial que sigue en aumento
y cuya solución es ya urgente. Cada vez se aíslan más bacterias y en más sitios
que son resistentes a varios antibióticos a la vez y, en algunos casos,
resistentes a todos los antibióticos disponibles, lo que supone un gran reto. A
esto hay que añadir el problema de que ya prácticamente ninguna empresa se
dedica a desarrollar nuevos antibióticos. (Ver nota “Resistencia a los antibióticos” de septiembre de 2016 de la OMS).
Un tipo de antibióticos muy interesante son los carbapenems porque, a diferencia de
otros antibióticos beta-lactámicos como las penicilinas, cefalosporinas y
monobactámicos, son de amplio espectro y resistentes a la mayoría de las beta-lactamasas. Por eso, los
carbapenems se suelen emplear en los casos graves, cuando la infección está
causada por una bacteria resistente a otros antibióticos y en infecciones
hospitalarias o nosocomiales. A veces a los carbapenems se los ha incluido
entre los antibióticos de “último recurso”.
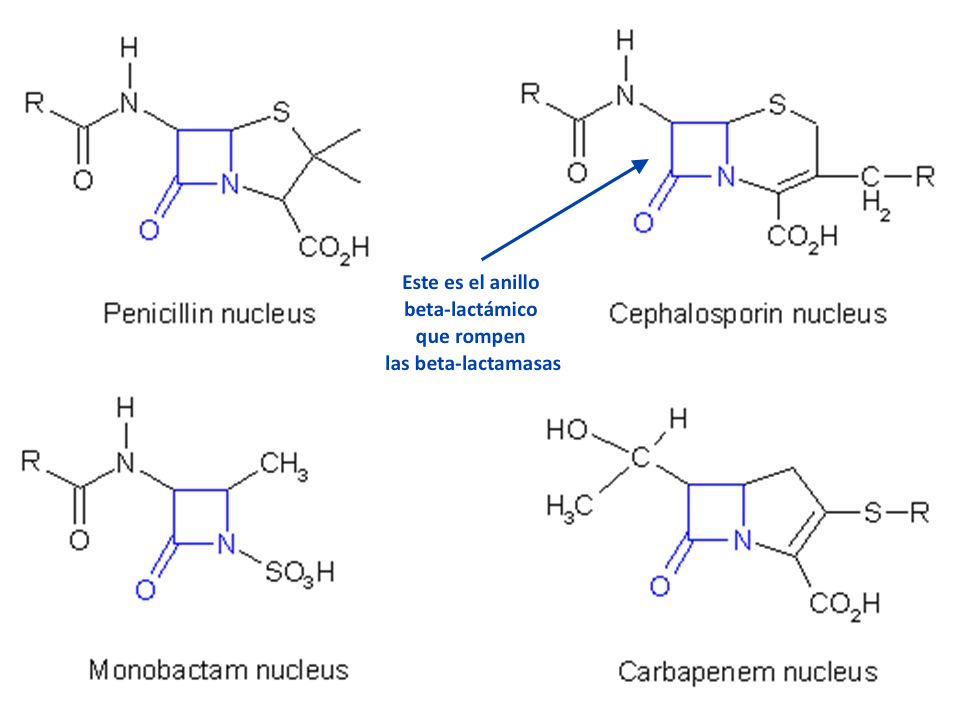
Las beta-lactamasas son enzimas que producen algunas
bacterias y que rompen el anillo
beta-lactámico de este tipo de antibióticos. De esta forma el antibiótico
pierde su actividad y la bacteria se hace resistente.
Sin embargo, existe una beta-lactamasa denominada NDM-1 (New Delhi metallo-beta-lactamase) que es particularmente peligrosa,
porque es capaz de romper también el anillo de los carbapenems. Confiere, por
tanto, resistencia a los carbapenems a la bacteria que la porta. Además, esta
beta-lactamasa está codificada en un plásmido
acompañada por otros genes que confieren resistencia a otros antibióticos. Como
los plásmidos se pueden intercambiar entre las bacterias, este tipo de resistencia
se extiende muy fácilmente entre el mundo bacteriano. Para colmo, la NDM-1 es
resistente a los inhibidores de las beta-lactamasas, como el ácido clavulánico.
Las bacterias portadoras del gen
NDM-1 son resistentes a los carbapenems
La primera vez que se detectó esta beta-lactamasa NDM-1 fue
en 2008 en la bacteria Klebsiella
pneumoniae aislada de un paciente sueco que se infectó en un viaje a la
India (de ahí en nombre de New Delhi, con el cabreo de las autoridades indias).
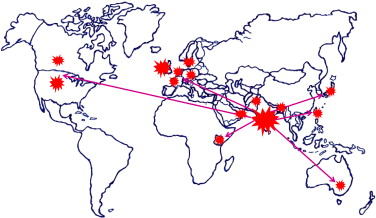
Debido a que esta beta-lactamasa está codificada por un plásmido y las
bacterias son muy promiscuas, desde entonces se ha aislado también en cepas de Escherichia coli, Pseudomonas aeruginosa y Acinetobacter
baumannii en más de 70 países por todo el planeta.
El problema, por tanto, es que el gen de resistencia a los antibióticos NDM-1 se extiende con mucha
facilidad entre las bacterias y es el responsable de la resistencia a los
carbapenems, unos antibióticos de “último recurso” muy útiles en aquello casos
de infecciones por bacterias resistentes a los antibióticos. Para solucionar
este problema, los investigadores se propusieron diseñar un compuesto capaz de inhibir la expresión del gen NDM-1 y
restaurar así la susceptible a los carbapenems en las bacterias portadoras de
dicho gen.
La solución
Han diseñado un compuesto denominado PPMO (Peptide-conjugated
Phosphorodiamidate Morpholino Oligomer), formado un pequeño fragmento de DNA
de unas 10-12 pares de bases unido (conjugado) a un péptido de argininas y
alaninas. Este compuesto reconoce unas secuencias reguladoras del gen NDM-1
donde se fija y bloquea su expresión. El PPMO inhibe, por tanto la síntesis de
la beta-lactamasa NDM-1.
PPMO es un inhibidor de la
expresión del gen de la beta-lactamasa NDM-1
Han probado que el PPMO es capaz de inhibir la síntesis de NDM-1 en varias bacterias resistentes a
los carbapenems: Escherichia coli,
Klebsiella pneumoniae y Acinetobacter baumannii. De esta forma,
al añadir el PPMO estás bacterias volvían a ser sensibles al antibiótico.

Halos de inhibición del crecimiento de E. coli NDM-1 resistente a los carbapenems alrededor de discos
impregnados con carbapenems (discos 1, 2 y 5) o con carbapenems + PPMO (discos
3, 4, 6 y 7). (Fuente referencia 1).
Además, han comprobado su efectividad in vivo. Para ello, han infectado ratones de laboratorio con
bacterias portadores del gen NDM-1 resistentes al carbapenem. Esas bacterias eran capaces de matar a los
ratones en menos de 18 horas, incluso aunque les administraran el antibióticos.
Sin embargo, cuando se les administraba el
antibiótico junto con el inhibidor PPMO, el 92% de los ratones eran capaces de vencer
la infección y sobrevivir.
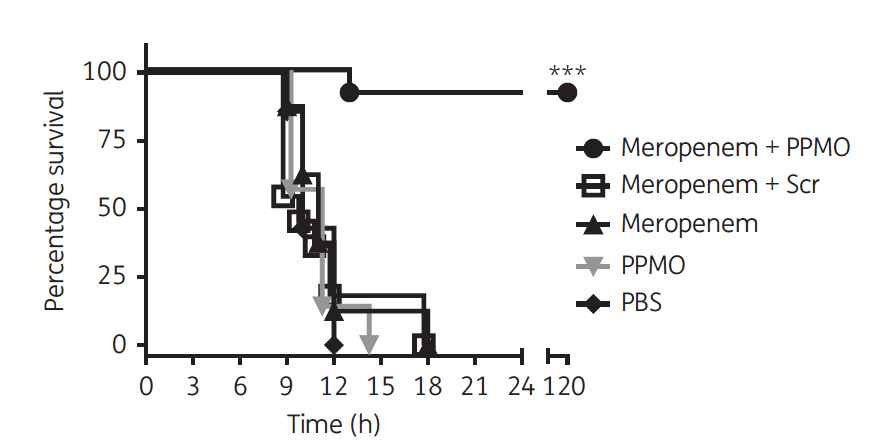
Efecto del inhibidor PPMO in vivo. Los ratones fueron infectado con la bacteria E. coli NDM-1 resistente a los
carbapenems. Solo los ratones que fueron tratados con el antibióticos
(meropenem) + el inhibidor PPMO sobrevivieron la infección (Fuente: referencia
1).
Esto demuestra que
este inhibidor PPMO puede ser empleado como agente terapéutico para combatir
las infecciones de bacterias NDM-1 resistentes a los carbapenems, … al menos en
ratones. Es una prueba de concepto muy prometedora, que pronto será ensayada en
humanos. Una nueva arma contra la resistencia a los antibióticos.
Y como microBIO cada vez se parece más a un video-blog, te dejo aquí con el resumen de #microBIOscope, la ciencia de microBIO en video, emitido vía Periscope y ahora editado para que lo puedas compartir en todas las redes sociales:
El resumen:
(1) Peptide-conjugated phosphorodiamidate morpholino oligomer (PPMO) restores carbapenem susceptibility to NDM-1-positive pathogens in vitro and in vivo. Sully EK, et al. J Antimicrob Chemother. 2016 Dec 20. pii:
dkw476. doi: 10.1093/jac/dkw476.








¡¡CIENCIA!! Siempre la CIENCIA :-))
Genial, me lo ha explicado muy bn.
Me alegro, gracias!